Vánoční pohádka o tom, proč má hořící svíčka štiplavou “vůni”
Lidský čich je poměrně nedokonalý. Přesto nás evoluce vybavila senzorem, který umí upozornit na existenci nepříliš zdravých substancí. Řada z nich pro nás voní podobně - jedná se například o halogeny, oxidy dusíku nebo ozón.
(obsahující chlor, fluor, chlor, brom nebo jód ve vosku svíček nenajdeme - halogenidy můžeme tedy zavrhnout. Zvláštní štiplavý zápach produkuje hořící svíčka díky vzniku určitého množství oxidů dusíku a tím i ozónu, který se může tvořit při rozpadu jednoho z nich. Největší podíl na zápachu svíček mají ovšem - oxidy dusíku.
Odkud se vzaly?
Svíčka má k dispozici hned dva zdroje. Jedním z nich je vzduch, druhým je samotný materiál svíčky.
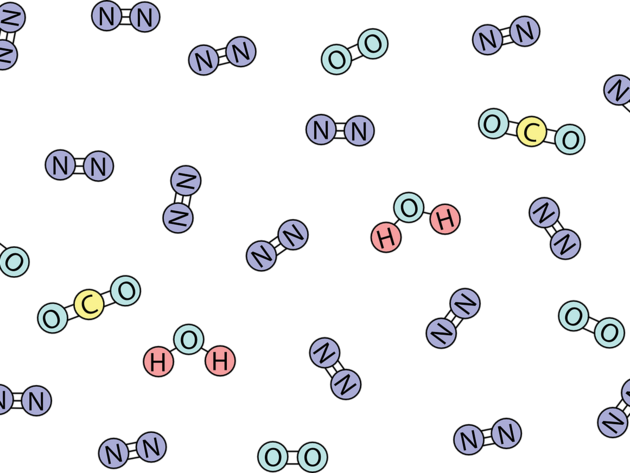
Vzduch je směs různých plynů. Nemalou část (kolem 78 objemových procent) z nich tvoří molekuly dusíku. Relativně lehký prvek vznikl v nitru obří hvězdy dávno před tím, než se z jejího popela vytvořila naše Sluneční soustava. Spolu s kyslíkem (nutným pro naše dýchání), křemíkem (z jehož sloučenin se skládá naše planeta) a uhlíkem (hlavní součástí živé hmoty) tvoří skupinu nejrozšířenějších prvků v našem okolí.
Spolu s vodíkem (nejrozšířenějším vesmírným prvkem) kdysi vytvořil molekuly čpavku - a právě v této podobě se kdysi dostal na Zemi spolu s ostatní hmotou komet, které ji v ještě mladé soustavě bombardovaly. První bakterie pak přeměnily čpavek na molekulární dusík.
Molekulární dusík
obsahuje dvě molekuly tohoto prvku. Je to bezbarvý plyn bez chuti a zápachu. Při velice nízkých teplotách mrzne na bezbarvý led (při -196°C). Ve vodě se rozpouští jen nerad (jen asi 23 ml v jednom litru vody při 0°C).
Lenivý dusík
Dusík sám o sobě je nehořlavý a co se týká jeho chemických aktivit - jsou jeho molekuly velice lenivé. Za chemické reakce je mimochodem zodpovědný elektronový obal látek a jeho uspořádání, kterému se říká odborně …
... elektronová konfigurace.
Elektrony, které má prvek k dispozici, obsazují určité předem dané orbitaly, které by se daly přirovnat k hotelovým pokojům.
Ty jsou dvoulůžkové - do každého se vejdou dva elektrony. Čím více elektronů prvek má, tím větší množství různých hotelových pokojů je jimi zaplněno. Podobně jako my lidé, ovšem bydlí elektrony rády v jednolůžkových pokojích. Poté, co bylo zaplněno první patro “atomárního hotelu”, stěhují se další elektrony do vyšších a vyšších pater. Ty, které obsadily poslední pokoje, bydlí o samotě. Jsou zpočátku spokojené. Jak to ale bývá i u lidí - po nějaké době se začnou nudit a je jim smutno. Hledají si nové partnery kde se dá - a podílejí se tak na chemických reakcích mezi prvky.
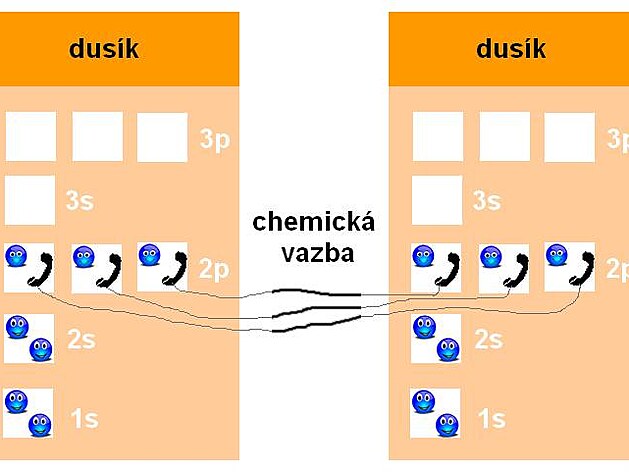
Pokud atom dusíku “potká” jiný atom dusíku - spřátelí se elektrony v jeho “2p” patře. Nemají pak už žádnou větší potřebu hledat si další partnery. Stačí jim, že si mohou se sousedy z vedlejšího hotelu telefonovat. Jak pokoje v prvním, tak druhém patře takové molekuly jsou obsazeny vcelku šťastnými elektrony. Atomární dusík je pak chemicky lenivý a nereaguje moc ochotně s jinými prvky. Oba atomy v molekule jsou vázány tzv. trojnou vazbou.
Pokud se chce jiný prvek seznámit s teď už spokojeným elektronem, který “telefonuje” se svým kolegou v jiném atomu dusíku - musí vynaložit daleko větší energii, než jaká vznikne jen pouhým klepáním na dveře. Musí ony pomyslné dveře doslova vylomit. V praxi to znamená, že na jeden mol látky se musí vynaložit 90 kJ energie. Tušíte správně. 90 kJ/mol energie se neválí jen tak na ulici. Může ji ale dodat například - hořící svíčka.
Pro srovnání - kdyby se stejná energie proměnila na kinetickou energii jednoho molu plynu (dusíku), odpovídalo by to rychlosti 2,6 km/s. Stejné množství energie proměněné na polohovou energii odpovídá zhruba výšce 340 km.
Druhým zdrojem oxidů dusíku je samotný materiál svíčky, lépe řečeno barviva, kterými se barví vosk. Ta ve své molekulární struktuře obsahují kromě běžného uhlíku vodíku a kyslíku často také dusík, který se při vyšší teplotě obzvláště rád mění na oxidy.
Svíčka zhotovená z bezbarvého vosku tedy vnáší do vzduchu “základní” znečištění, zatímco barevné svíčky zásobují náš vzduch mnohanásobně větším množstvím oxidů dusíku.
V dobře větraných (starých) stavbách to jistě není problém. Pokud ale vychutnáváte větší množství svíček v bytě s moderními okny, které dobře těsní, na závěr jistě neuškodí krátké vyvětrání.
Co přesně se děje během hoření?
Energie, kterou dodává plamen, stačí na to, aby proběhla chemická reakce - oxidace původně spokojeného a lenivého dusíku. Tato energie (ne nepodobná zemětřesení) přetrhá pomyslné telefonní vedení všem elektronům v nejvyšším patře atomárního hotelu. V následujícím chaosu se už nespárují s jiným atomem dusíku - ale s atomem kyslíku.
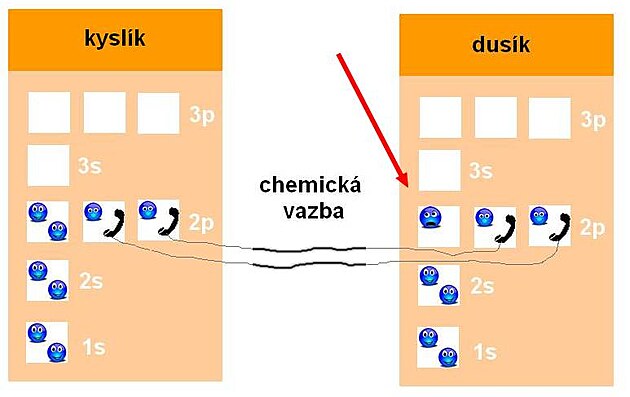
Kyslík má trochu jinou elektronovou konfiguraci než dusík. Vždyť každý prvek má své vlastní specifické množství protonů v jádře - a proto také vlastní počet elektronů, které náboj z jádra vyvažují, aby byl atom elektricky neutrální. Kyslík má na rozdíl od dusíku ne sedm - ale hned osm elektronů. Dva z nich jsou chronicky “nešťastné”.
Oba se chtějí spárovat s elektrony z jiných atomů. Při spojení dusíku a kyslíku do molekuly oxidu dusnatého (N=O) vzniká ale jen další - a zase poměrně nešťastná sloučenina. Má totiž pořád ještě jeden nespárovaný elektron, který se pokouší sehnat nějakého přítele (na obrázku zvýrazněný červenou šipkou).
Naštvaný, nešťastný a psychicky nevyvážený elektron způsobuje v praxi řadu problémů. Oxid dusnatý je metastabilní. Při nízkých teplotách se snaží svoje dilema řešit tím, že sdružuje dvě molekuly N=O do dočasného manželství - dimerizuje. Smutné elektrony obou molekul si sice nemohou telefonovat, ale alespoň si píší maily.
Při vysokých teplotách N=O naopak oxiduje a vytváří oxid dusičitý (O=N=O). Ale ani tento experiment ho neuspokojuje - prostě to není ono. NO2 dimerizuje (tvoří dvoumolekulu) ještě raději než N=O. Ovšem už při teplotách kolem -11°C se dimer zase rozpadá. Při teplotě kolem 150 °C se mu zase začíná stýskat po existenci ve formě N=O a při 600°C už se na něj přeměnil úplně. Oxid dusíku zkrátka není nikdy dostatečně spokojený.
Každý solidní a slušný atom dusíku doufá, že se jednoho dne zase bude smět spárovat se svým nejmilejším příbuzným … jiným atomem dusíku.
V praxi to znamená, že reakce, které pozorujeme při oxidaci dusíku, jsou vratné a probíhají oběma směry. Parametrem, který určuje momentální koncentraci toho či onoho oxidu je především teplota.
Následující tabulka ukazuje závislost koncentrace N=O na okolní teplotě. V levém sloupečku je zanesená teplota, v pravém sloupečku se nachází koncentrace v objemových procentech.
| 200 | 10-7 |
|---|---|
| 700 | 0,04 |
| 1200 | 0,1 |
| 1800 | 0,5 |
| 1900 | 1 |
Teoreticky by se tedy měl oxid N=O při odchodu z horké zóny plamene svíčky zase rozpadnout. Už při teplotě 200°C by měla být jeho koncentrace jen minimální.
V praxi se to neděje. Zjevně je pro molekulu N=O lepší vrabec v hrsti než holub na střeše - zůstává tedy ve svém neuspokojivém stavu. Chemik takové chování nazývá metastabilní. K rozpadu je potřeba dodat určitou energii, která dostala příznačné jméno “aktivační”.
Přesně to je důvod pro existenci oxidu dusíku v našem obýváku - a také pro štiplavou vůni svíček.
Oxid dusíku se díky energii dodané svíčkou sice vytvoří, ale nemá dost slušnosti, aby se zase hned rozpadl.
Něco podobného se děje mimochodem také na silnicích. U aut, která používají spalovací motory totiž vznikají oxidy dusíku stejně, jako v případě hořící svíčky. Zatímco u svíček se proti tomu nedá nic moc podniknout - vymyslel automobilový průmysl částečnou pomoc. Vysoká hodnota aktivační energie (potřebné k rozložení N=O na původní komponenty) se snižuje pomocí katalyzátorů.
Dana Tenzler
Alkohol v jídle - kolik se ho vypaří během vaření?

Odpařuje se alkohol, který se přidává do jídla, během vaření natolik, aby byl výsledný pokrm vhodný pro děti? O alkoholu v potravinách. (délka blogu 4 min.)
Dana Tenzler
Barvy v kuchyni (8) - průmyslová modrá

Napadlo vás někdy, čím se vlastně barví potraviny? Jakými přírodními nebo umělými barvivy se dá jídlo barvit dnes a jak tomu bylo v minulosti? (délka blogu 3 min.)
Dana Tenzler
Barvy v kuchyni (7) - přírodní modrá

Napadlo vás někdy, čím se vlastně barví potraviny? Jakými přírodními nebo umělými barvivy se dá jídlo barvit dnes a jak tomu bylo v minulosti? (délka blogu 3 min.)
Dana Tenzler
Barvy v kuchyni (6) - průmyslová zelená

Napadlo vás někdy, čím se vlastně barví potraviny? Jakými přírodními nebo umělými barvivy se dá jídlo barvit dnes a jak tomu bylo v minulosti? (délka blogu 3 min.)
Dana Tenzler
Barvy v kuchyni (5) - přírodní zelená

Napadlo vás někdy, čím se vlastně barví velikonoční vajíčka? Jakými přírodními nebo umělými barvivy se dá jídlo barvit dnes a jak tomu bylo v minulosti? (délka blogu 3 min.)
Dana Tenzler
Barvy v kuchyni (4) - průmyslová červená

Blíží se Velikonoce. Napadlo vás někdy, čím se vlastně barví velikonoční vajíčka? Jakými přírodními nebo umělými barvivy se dá jídlo barvit dnes a jak tomu bylo v minulosti? (délka blogu 3 min.)
Dana Tenzler
Barvy v kuchyni (3) - přírodní červená

Blíží se Velikonoce. Napadlo vás někdy, čím se vlastně barví velikonoční vajíčka? Jakými přírodními nebo umělými barvivy se dá jídlo barvit dnes a jak tomu bylo v minulosti? (délka blogu 3 min.)
Dana Tenzler
Barvy v kuchyni (2) - průmyslová žlutá

Blíží se Velikonoce. Napadlo vás někdy, čím se vlastně barví velikonoční vajíčka? Jakými přírodními nebo umělými barvivy se dá jídlo barvit dnes a jak tomu bylo v minulosti? (délka blogu 3 min.)
Dana Tenzler
Barvy v kuchyni (1) - přírodní žlutá

Blíží se Velikonoce. Napadlo vás někdy, čím se vlastně barví velikonoční vajíčka? Jakými přírodními barvivy se dá jídlo barvit dnes a jak tomu bylo v minulosti? První díl seriálu o barvách.
Dana Tenzler
Čokoládoví velikonoční zajíčci

Blíží se Velikonoce. Napadlo vás někdy, odkud se vlastně vzali velikonoční zajíčci a vajíčka z čokolády, kterých jsou před velikonocemi plné obchody? (délka blogu 3 min.)
Dana Tenzler
První lidé, kteří přišli do Evropy - nové datování hornin

Nedávno proběhla médii zpráva o tom, že lidstvo začalo osídlovat Evropu z východu kontinentu. Jak ale vědci určili stáří vzorků? Na datování pomocí radioaktivních izotopů uhlíku totiž byly moc staré. (délka blogu 5 min.)
Dana Tenzler
Umělé zatmění Slunce

ESA se chystá vytvořit (s pomocí dvou satelitů) první umělé zatmění Slunce. Nový převratný experiment na oběžné dráze Země. (délka blogu 3 min.)
Dana Tenzler
Budoucnost života na Zemi (4) - vliv Měsíce

Poslední díl malého seriálu o budoucnosti života na Zemi. Může naši planetu zachránit vliv Měsíce? Shrnutí a statistika počítačových simulací. (délka blogu 3 min.)
Dana Tenzler
Budoucnost života na Zemi (3) Záchrana díky cizí hvězdě?

Planeta Země se nyní nachází v obyvatelné zóně Slunce. Taková zóna existuje kolem každé hvězdy. Planeta se v ní ale nemusí udržet věčně. (délka blogu 5 min.)
Dana Tenzler
Budoucnost života na Zemi (2) Klima na budoucím superkontinentu

Jak se vyrovnají savci se změnami klimatu na budoucím superkontinentu Pangea Ultima? Už dnes známe jejich budoucí strategii. (délka blogu 3 min.)
Dana Tenzler
Budoucnost života na Zemi (1)

To, že se naše planeta nachází v obyvatelné části Sluneční soustavy, považujeme za samozřejmé. Samozřejmé to ale není. V budoucnosti proběhnou změny, které život na Zemi vyhubí. Seriál blogů o budoucím vývoji Země. (délka 4 min.)
Dana Tenzler
?Podaří se další přistání na Měsíci? Intuitive Machines

Dalším účastníkem nového závodu o Měsíc je americká soukromá firma Intuitive Machines. Její sonda se dnes bude pokoušet o měkké přistání na Měsíci. (délka blogu 2 min.)
Dana Tenzler
Objev první temné galaxie

Vědci nedávno zveřejnili objev zvláštní galaxie. Pozorovali ji v rádiové oblasti elektromagnetického spektra. Přitom si všimli, že v ní nejspíš ... úplně chybí hvězdy. (délka blogu 2 min.)
Dana Tenzler
Vulkány na Jupiterovu měsíci Io

NASA zveřejnila nové snímky nejbližšího Jupiterova měsíce - Io. Zachytila je vesmírná sonda Juno, která se už nejspíš blíží ke konci své aktivní činnosti. (délka blogu 3 min.)
Dana Tenzler
Satelit CUTE a jeho průzkum „horkých Jupiterů“

Maličký satelit s velikostí krabice od bot (třídy cube 6U, tedy 6x10x10x10 cm) se věnuje zajímavému průzkumu. Doplňuje naše znalosti o zvláštním typu exoplanet, který se nevyskytuje ve Sluneční soustavě. (délka blogu 3 min
| předchozí | 1 2 3 4 5 6 7 ... | další |
- Počet článků 968
- Celková karma 19,29
- Průměrná čtenost 1331x